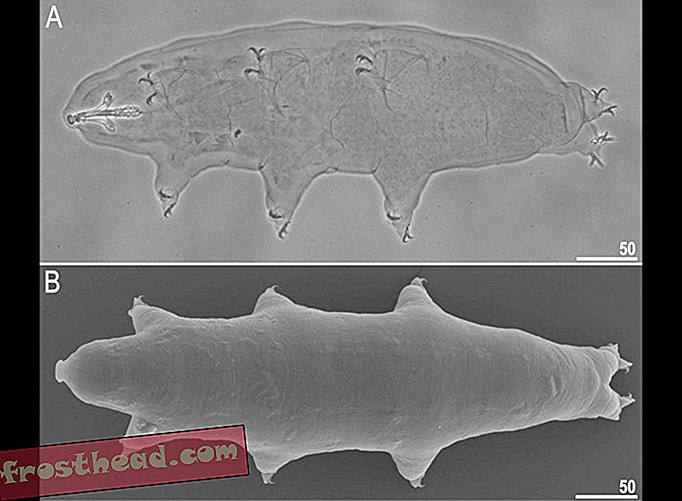
Selle nädala uus uuring on tõmbanud geenide redigeerimise piirid, näidates taas, et teadlased suudavad nüüd edukalt parandada inimeste embrüote teatud haigusi põhjustavaid mutatsioone. Eile ajakirjas Nature avaldatud tulemused kogusid palju pealkirju, uudised kolimisest lekkisid isegi eelmise nädala alguses. Ehkki tegemist pole inimembrüo redigeerimise esimese juhtumiga, on see teadaanne uuesti süüdanud poleemika geenide redigeerimise eetika üle. Siin on viis asja, mida peaksite selle värskeima uuringu kohta teadma.
1. CRISPR lööb uuesti
Selles uuringus töötasid teadlased geenide redigeerimise süsteemiga CRISPR-Cas9, mis on nagu geenide lõikamine ja kleepimine. See põhineb looduslikult esineval immuunsussüsteemil, mida leidub paljudes bakteriliikides ja milles mikroobid peavad genoomis viiruse DNA nimistut, et nad tunneksid ära tulevased ohtlikud sissetungijad. Kui seda DNA-d leidub, siis kasutavad bakterid ensüüme nimega Cas (CRISPR-ga seotud valgud), mis need DNA-d täpselt ja tõhusalt välja lõhustavad.
Viimases uuringus kasutasid teadlased seda tööriista geeni MYBPC3 mutatsiooni eemaldamiseks, mis põhjustab südamelihase paksenemist - potentsiaalselt surmaga lõppevat seisundit, teatas Emily Mullin MIT Technology Review-st . Pärast selle edukat väljalõikamist kopeerisid nad tervisliku versiooni viilutatud sektsiooni.
2. See ei ole esimene inimembrüote omamoodi redigeerimine
See uuring oli tähelepanuväärne elujõuliste embrüote või embrüote kasutamise osas, mis kasvades võiksid tõenäoliselt areneda beebiks, teatas Dina Fine Moran ajakirjale Scientific American . See on esimene kord, kui seda kunagi USA pinnal juhtub, kuid Hiina teadlased on juba aastaid ümbrikku surunud. Aastal 2015 moodustas rühm Hiina teadlasi esimest korda geneetiliselt muundatud embrüoid. Ja selle aasta alguses muutis teine teadlaste rühm esmakordselt elujõuliste embrüote geene.
USA valitsusel ja tema sidusettevõtetel, sealhulgas suurtel regulaatoritel nagu toidu- ja ravimiamet, keelatakse rahastada teadusuuringuid, mis hõlmavad inimese embrüoid, st teadlased pidid selle uuringu jaoks kasutama era- või institutsionaalseid vahendeid, vahendab Heidi Ledford for Nature . Veebruaris avaldatud aruanne avas ettevaatlikult ukse võimalikule USA valitsuse võimalikule embrüogeeni redigeerimise uuringute rahastamisele, kuid pole selge, millal see soovitus määrustesse saab.
3. Järgmine samm võib kolida välismaale
Selle uurimistöö järgmine samm on välja selgitada, kas sel viisil modifitseeritud embrüod võivad tegelikult tervislikult kasvada, vahendab The Guardian Ian Sample. Kuid USA keelab rangelt sellist laadi kliinilised uuringud ja ei tundu tõenäoline, et reeglid peagi muutuvad.
"Ees on veel pikk tee, " räägib uuringu autor Shoukhrat Mitalipov Näidisele. "Pole selge, millal lubatakse meil edasi liikuda."
Edasiliikumiseks võivad teadlased vajada suunamist kuskile lubavamale, teatab Kate Lunau Vice Motherboardist . "Me toetaksime selle tehnoloogia kolimist erinevatesse riikidesse, " räägib Mitalipov Lunaule.
4. Seal on poleemikat
Eilsete teadusuuringute uudistega kaasnes arvukalt mõtteid ja toimetusi, kus paljud väljendasid muret selle üle, kui kaugele see teadusuuring teadust tundmatule territooriumile viib, ning nõuavad ettevaatust.
"Geeniredaktsiooni ohutusest ei tea me liiga palju, et insenertehnilised inimesed, kes suudavad mutatsioone edastada, rändaksid mööda Maad. Millised on isegi kergete redigeerimisvigade potentsiaalsed tervisemõjud? Me ei tea veel, " rääkis Alessandra Potenza kirjutab The Verge'i jaoks raportist, mille eile avaldas rahvusvaheline geneetikute rühm.
"Avalik kord ja bioeetika pole geneetilise sekkumise teadusega järele jõudnud, " kirjutab Los Angeles Timesi toimetus. "On ülimalt tähtis, et saaksime inimese geenide redigeerimise õigeks, mitte ainult varsti."
Teised võitlesid uudise vastu kui lootuse pakkumist pärilike haigustega võitlejatele. Siia kuulub ka Alex Lee, kes kannatab Leberi päriliku optilise neuropaatia all, mis on haruldane mitokondriaalne haigus. Ta kirjutab ajalehele The Guardian:
"Neil, keda geneetilised haigused ei mõjuta, on lihtne loobuda teaduse arengust sammuna tuleviku suunas, kus hakkame silma- või juuksevärvi kriteeriumi valima kujundus-ise-beebide kataloogist. Kuid minusuguste inimeste jaoks, keda mõjutab ravimatu geneetiline haigus, mis pani mind pimedaks minema, ei paku teaduslikud edusammud geenide redigeerimise ja mitokondriaalse asendusravi jaoks midagi muud kui lootust. "
5. Me ei kavanda beebisid (veel)
"Sellest on laialt teatatud kui disaineri beebi ajastu algusajale, mistõttu on sellest tõenäoliselt juba viiendat või kuuendat korda teada antud koidik, " räägib bioeetik Alta Charo Theatreist Ed Yongile. "Ja see pole nii."
Esiteks, teatab Megan Molteni Wiredist, on lapsele tahtmatute tunnuste valimine tegelikult palju keerulisem kui see protsess. Selle uuringu teadlased võtsid ühe geeni ja modifitseerisid seda embrüo juurde jõudmiseks, et kopeerida muteeritud geeni asemel terve DNA järjestus.
“Kõik räägivad alati geenitoimetamisest. Mulle ei meeldi sõna redigeerimine. Me ei muutnud ega muutnud midagi, ”räägib Mitalipov Moltenile. "Kõik, mida me tegime, oli modifitseerimata mutantgeen, kasutades olemasolevat metsiktüüpi ema geeni."
Selliseid tunnuseid nagu kõrgus, juuste värv ja silmade värv on juhitud sadade või tuhandete erinevate geenide abil viisil, millest teadlased veel täielikult aru ei saa. Ja need vajaksid splaissimist täiesti uutes DNA järjestustes, mis tuleks luua või teistelt inimestelt tõmmata. Sellegipoolest näevad teadlased tulevikku, kus seda võiks arutada, ja loodavad seda mõistlikult kontrollida.
"On mure, et seda võiks kasutada täiustamiseks, seega peab ühiskond tõmbama piiri, " räägib Mitalipov Yongile. "Kuid see on üsna keeruline tehnoloogia ja seda poleks keeruline reguleerida."